
دهه های متمادی پژوهش و تجربه بالینی ما را به عصر جدیدی از مدیریت بهینه اختلالات موکوپلی ساکاریدوز (MPS) رسانده است. این استاندارد مراقبتی MPS که با سرعت در حال پیشرفت است، متکی به یک متخصص ژنتیک در مرکزیت مدل ارائه مراقبت های درمانی است که می تواند مراقبت های هماهنگ چندرشته ای را فراهم کرده و فرصت بی نظیری برای تغییر زندگی بیماران به پزشکان می دهد.1–3
ماهیت ناهمگن و متغیر اختلالات MPS نیاز به رویکردهای شخصی در مراقبت های هماهنگ بیماران را مطرح می سازد که از مرکز پزشکی آغاز می گردد.4 هدف مراقبت های هماهنگ کمک به بیماران در دست یافتن به کیفیت زندگی بهتر است که شامل این موارد می باشد:
در مورد کودکان مبتلا به بیماری های حاد، پیچیده و مولتی سیستمیک ژنتیک مانند MPS، مراقبت توسط یک مرکز پزشکی هماهنگ می تواند از نیاز به استفاده از مراقبت های درمانی کاسته و نتایج سلامتی را بهبود بخشد.5
هماهنگی باید در تمام مؤلفه های یک سیستم جامع درمانی (مانند مراقبت های تخصصی، بیمارستان ها، مراقبت های بهداشتی خانگی و خدمات اجتماعی) و در برنامه های شخصی مدیریت بیماران اجرا گردد.3 نقش متخصص ژنتیک و/یا متخصص بیماری های متابولیک در اجرای بهترین شیوه های مدیریت ممکن برای اختلالات MPS و بهبود نتایج برای بیماران می تواند تعیین کننده باشد.1,2
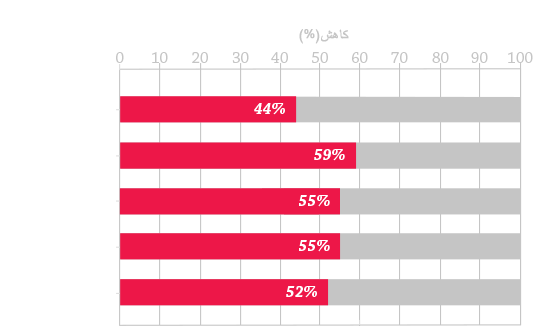
اعمال مدیریت بهینه بیماری MPS با در نظر گرفتن سه اصل مراقبت زیر می تواند به بهبود نتایج برای بیماران کمک کند:

متخصصان ژنتیک و/یا متخصصان بیماری های متابولیک بعنوان متخصصان پزشکی که دانش و اطلاعات گسترده ای درباره اختلالات ژنتیک مانند MPS دارند، نقش بسیار مهمی در هماهنگی برنامه های مدیریت فردی ایفا می نمایند که به ERT، مدیریت در کل عمر و مراقبت های رویه ای پرداخته و می توانند در بهبود نتایج برای بیماران مفید واقع شوند.1,2
ERT، در صورت وجود اساس و بنیاد درمان را تشکیل می دهد.9,10
اگرچه هریک از زیرگروه های اختلالات MPS از لحاظ بالینی متفاوت هستند اما تمام آنها دارای خصوصیات کوتاه کننده عمر، پیشروندگی و تظاهرات مولتی سیستمیک مشترک در پاتولوژی بیماری MPS می باشند.11,12,21,22 مدیریت بیماران مبتلا به MPS نیاز به درک تظاهرات خاص بالینی و توصیه های مدیریتی برای هریک از زیرگروه های MPS دارد.2,10
نوامبر 2015
علیرغم تنظیمات متعدد امکان بیهوشی بهینه دوطرفه زایمان نبود و برای عمل سزارین نیاز به بیهوشی سیستمیک بود.
می 2015
تشخیص به دلیل عدم وجود یا فاصله زیاد با مراکز و امکانات تشخیصی با تأخیر روبرو شد و منجر به تشخیص های دیگر و علائم گمراه کننده گردید. تعدادی از بیماران تظاهرات و علامت هائی را تجربه کردند که از آنچه که انتظار می رفت کم رنگ تر بودند ولذا مد نظر قرار داده نشدند. این موارد همچنین چالش های منحصر بفردی را نشان می دهند که در تشخیص MPS VI توسط تخصص های مختلف وجود دارد و مطالبی درباره تظاهرات اولیه این بیماران ارائه می کنند.
آوریل 2016
اطلاعات ما درباره سایر مسائل قلبی در میان بزرگسالان مبتلا به MPS، بخصوص در زمینه گردش خون در عروق کرونر و ميوکاردیوم ناچیز است و برای اینکه بتوانیم مراقبت های موثری از این جمعیت نوظهور بزرگسالان بعمل آوریم نیاز به دانش و اطلاعات بیشتر است.
References: 1. Hendriksz CJ, Berger KI, Giugliani R, et al. International guidelines for the management and treatment of Morquio A syndrome. Am J Med Genet Part A. 2014;9999A:1–15. doi:10.1002/ajmg.a.36833. 2. Muenzer J. The mucopolysaccharidoses: a heterogeneous group of disorders with variable pediatric presentations. J Pediatr. 2004;144(suppl 5):S27–S34. 3. Agency for Healthcare Research and Quality. Defining the PCMH. https://pcmh.ahrq.gov/page/defining-pcmh. Accessed December 15, 2015. 4. Hendriksz CJ, Harmatz P, Beck M, et al. Review of clinical presentation and diagnosis of mucopolysaccharidosis IVA. Mol Genet Metab. 2013;110:54–64. doi:10.1016/j.ymgme.2013.04.002. 5. Casey PH, Lyle RE, Bird TM, et al. Effect of hospital-based comprehensive care clinic on health costs for Medicaid-insured medically complex children. Arch Pediatr Adolesc Med. 2011;165(5):392–398. doi:10.1001/archpediatrics.2011.5. 6. Mosquera RA, Avritscher EBC, Samuels CL, et al. Effect of an enhanced medical home on serious illness and cost of care among high-risk children with chronic illness: a randomized clinical trial. JAMA. 2014;312(24):2640–2648. doi:10.1001/jama.2014.16419. 7. Klitzner TS, Rabbitt LA, Chang RKR. Benefits of care coordination for children with complex disease: a pilot medical home project in a resident teaching clinic. J Pediatr. 2010;156(6):1006-1010. doi:10.1016/j.jpeds.2009.12.012. 8. Gordon JB, Colby HH, Bartelt T, Jablonski D, Krauthoefer ML, Havens P. A tertiary care-primary care partnership model for medically complex and fragile children and youth with special health care needs. Arch Pediatr Adolesc Med. 2007;161(10):937–944. 9. Hendriksz C. Improved diagnostic procedures in attenuated mucopolysaccharidosis. Br J Hosp Med. 2011;72(2):91–95. 10. Muenzer J, Wraith JE, Clarke LA, International Consensus Panel on the Management and Treatment of Mucopolysaccharidosis I. Mucopolysaccharidosis I: management and treatment guidelines. Pediatrics. 2009;123(1):19–29. doi:10.1542/peds.2008-0416. 11. Muenzer J. Overview of the mucopolysaccharidoses. Rheumatology (Oxford). 2011;50(suppl 5):v4-v12. 12. Lehman TJA, Miller N, Norquist B, Underhill L, Keutzer J. Diagnosis of the mucopolysaccharidoses. Rheumatology. 2011;50(suppl 5):v41–v48. 13. Kakkis ED, Neufeld EF. The mucopolysaccharidoses. In: Berg BO, ed. Principles of child neurology. New York, NY: McGraw-Hill; 1996:1141–1166. 14. Lavery C, Hendriksz C. Mortality in patients with Morquio syndrome A. J Inherit Metab Dis Rep. 2015;15:59–66. doi:10.1007/8904_2014_298. 15. Giugliani R, Lampe C, Guffon N, et al. Natural history and galsulfase treatment in mucopolysaccharidosis VI (MPS VI, Maroteaux-Lamy syndrome) – 10-year follow-up of patients who previously participated in an MPS VI Survey Study. Am J Med Genet A. 2014;164A(8):1953–1964. doi:10.1002/ajmg.a.36584. 16. Spinello CM, Novello LM, Pitino S, et al. Anesthetic management in mucopolysaccharidoses. ISRN Anesthesiol. 2013;2013:1–10. doi:10.1155/2013/791983. 17. Sam JA, Baluch AR, Niaz RS, Lonadier L, Kaye AD. Mucopolysaccharidoses: anesthetic considerations and clinical manifestations. Middle East J Anaesthesiol. 2011;21(2):243–250. 18. Data on file. Biomarin Pharmaceutical, Inc. 19. Drummond JC, Krane EJ, Tomatsu S, Theroux MC, Lee RR. Paraplegia after epidural-general anesthesia in a Morquio patient with moderate thoracic spinal stenosis. Can J Anesth. 2015;62(1):45–49. doi:10.1007/s12630-014-0247-1. 20. Sharkia R, Mahajnah M, Zalan A, Sourlis C, Bauer P, Schöls L. Sanfilippo type A: new clinical manifestations and neuro-imaging findings in patients from the same family in Israel: a case report. J Med Case Rep. 2014;8:78. doi:10.1186/1752-1947-8-78. 21. Clarke LA, Winchester B, Giugliani R, Tylki-Szymańska A, Amartino H. Biomarkers for the mucopolysaccharidoses: discovery and clinical utility. Mol Genet Metab. 2012;106(4):396–402. doi:10.1016/j.ymgme.2012.05.003. 22. Morishita K, Petty RE. Musculoskeletal manifestations of mucopolysaccharidoses. Rheumatology. 2011;50(suppl 5):v19–v25. doi:10.1093/rheumatology/ker397. 23. Ashworth JL, Biswas S, Wraith E, Lloyd IC. Mucopolysaccharidoses and the eye. Surv Ophthalmol. 2006;51(1):1–17.