
موکوپلی ساکاریدوز (MPS) IV یا سندروم مورکیو یک اختلال پیشرونده و مولتی سیستمیک ذخیره سازی لیزوزومی ناشی از کمبود آنزیم های ان-استیل گلوکز آمين 6-سولفاتاز یا بتا-گالاکتوسیداز مسئول فروگشت گلیکوز آمینو گلیکان ها (GAGها) است2 که در ساخت استخوان ها، غضروف، پوست، تاندون ها و بسیاری دیگر از بافت های بدن نقش دارند.3 دو نوع مشخص آن شناخته شده اند: نوع A (MPS IVA، مورکیو نوع A) و نوع B (MPS IVB). اینها در عامل ژنتیک بوجود آورنده بیماری با هم تفاوت دارند، اما علائم و نشانه های این نوع ها می تواند شبیه بوده و در روند پیشرفت بیماری ظاهر می شوند.4
MPS IV یک عارضه پیشرونده، مولتی سیستمیک و برای تمام عمر است که می تواند به بیماری های سیستمیک و کوتاه شدن عمر منجر گردد.1
تصور رایج از نادر بودن بیماری، تظاهرات ناهمگان و تنوع و تغیر در تظاهرات بیماری تشخیص آنرا دشوار ساخته و بر اهمیت مداخله زودهنگام صحه می گذارد.1 فارغ از فنوتیپ، علائم می توانند تا آسیب نهائی اندام پیش بروند. عوامل ریسک برای بالا رفتن احتمال مرگ عبارتند از:4,5
اکثریت بیماران مبتلا به مورکیو نوع A بیشتر از دو دهه زندگی نمی کنند و عوامل اصلی مرگ عبارتند از نارسائی تنفسی، عوارض جراحی و نارسائی قلبی.1
بیماران مبتلا به MPS IV، که عمدتاً یک عارضه عضلانی استخوانی شناخته می شود،1 ممکن است علائمی غیرقابل پیش بینی و از لحاظ بالینی ناهمگن جدای از تظاهرات فوق داشته یا در آنها پدیدار شود.6 جدول زیر نشان دهنده علائم و نشانه های احتمالی مورکیو نوع A است که ممکن است به تنهائی یا در کنار سایر علائم مشاهده گردند و در صورت برخورد باید به مورکیو نوع A شک کنکید.
تظاهرات پیشرونده و سیستمیک می توانند منجر به تبعات احتمالاً وخیم قلبی عروقی،1,7–9 ریوی، 1,6,7,10,11 عصبی،6,12 عضلانی استخوانی،1,6 روماتولوژیک،5,13 چشمی،1,14,15 گوش، حلق و بینی،1,16 کبدی/شکمی،13 و دندانی6,17 شوند. البته باید توجه داشت که بیماران مبتلا به MPS IV برخلاف سایر اختلالات MPS دارای ناتوانی شناختی نیستند.
لازم به ذکر است که بیش از 70% بیماران در نخستین 2 تا 3 سال زندگی خود خصوصیات غیرعادی استخوانی خواهند داشت.6 در مطالعات اخیر عنوان شده است که حدود 25% بیماران مبتلا به سندروم مورکیو نوع A دارای فنوتیپ غیرکلاسیک هستند.5
بیماران ممکن است الگوی کلاسیک یا غیرکلاسیک علائم و نشانه ها را داشته باشند. در مورد بیمارانی که فنوتیپ غیرکلاسیک را دارند اغلب گزارش می شود که زمان رسیدن به تشخیص به نسبت شروع علائم با تأخیر قابل توجهی روبروست.1 پیشرفت متغیر بیماری در بیماران مبتلا به مورکیو نوع A18 
فارغ از فنوتیپ،1 علائم می توانند به آسیب هائی مرحله نهائی اندام منجر شوند.
بی توجهی به تظاهرات غیرکلاسیک مورکیو نوع A می تواند باعث عدم تشخیص یا تأخیر تشخیص شده و تبعات قابل توجهی را به دنبال داشته باشد:
ملاحظات جراحی نیاز به جراحی و گستردگی آن در میان بیماران مبتلا به مورکیو نوع A بالاست. بر اساس یک مطالعه تاریخچه سیر طبیعی مورکیو نوع A، 70% جمعیت (سن متوسط 14.5 سال) حداقل 1 عمل جراحی داشته اند.7
تاریخچه جراحی بیماران و نیاز آنها به آنها جراحی هم باید ذهن شما را به احتمال IV MPS سوق دهد.
مورکیو نوع A و MPS IVB به دلیل موتاسیون ژن های GALNS و GLB1 رخ می دهد که به ترتیب آنزیم های ان-استیل گلوکز آمين 6-سولفاتاز و بتا-گالاکتوسیداز را کدگذاری می نمایند.1,25 کمبودهای آنزیمی ناشی شده منجر به پاتولوژی های متعدد متابولیک می شود که از میان مهم ترین آنها می توان به انباشت سوبستراهای GAG کراتان سولفات و کندروایتین-6-سولفات در لیزوزوم های سراسر بدن اشاره کرد.1,26
با انباشته شدن لیزوزوم ها آنها فضای بیشتری را در سیتوپلاسم اشغال کرده و ارگانل های آنها را پوشانده و باعث اخلال در عملکرد می شوند.27 نقص عملکرد آنزیمی در MPS IV منجر به نارسائی کارکردی سلول ها، بافت و سیستم های اندام شده و باعث بیماری پیشرونده مولتی سیستمیک می شود که جزو خصائص این اختلال است.1,6 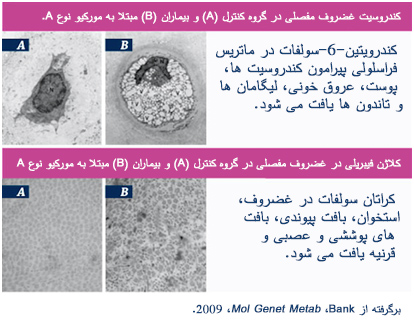
مطالعات و تحقیقات مستمر به بهبود کیفیت مدیریت وضعیت بیماران منجر شده است:
استاندارد مراقبت های مورکیو نوع A در متن "معیارها و موازین بین المللی مدیریت و درمان سندروم مورکیو نوع A" که در سال 2014 منتشر شد تعریف شده است. به دلیل ماهیت پیشرونده بیماری، بر شروع سریع درمان ERT در این معیارها تأکید شده است.
علاوه بر ERT، مدیریت در طول عمر و مراقبت های رویه ای از یک گروه مراقبت های هماهنگ چندرشته ای نیز برای بهینه ساختن نتایج برای بیمار اهمیت بسیار زیادی دارند.6 مراقبت های حمایتی شامل دارو و مداخله های جراحی، شامل این موارد می باشد:1,6,7
به دلیل ماهیت غیرقابل پیش بینی و مولتی سیستمیک MPS IVA، برای شناسائی علائم آسیب در اندام ها و تضمین نتایج بهینه برای بیماران نیاز به معاینات و درمان های مرتب، چندرشته ای و جامع یک گروه مراقبتی هماهنگ می باشد.1,6 پزشکان می توانند با تهیه برنامه های مدیریت شخصی برای هریک از بیماران خود، مدیریت وضعیت بیماران را بهینه ساخته و کار را با یک برنامه ارزیابی های جامع برای تمام سیستم های بدن که تحت تأثیر MPS IVA هستند شروع نمایند.1
پس از تأیید تشخیص، ارزیابی های تعیین خط مرجع باید انجام شده و فوراً ERT آغاز گردد. ERT می تواند استقامت جسمانی را بر اساس سنجش های 6MWT به میزان قابل توجهی بهبود ببخشد. تغییر قابل توجه 6MWT بیانگر بهبود یا تشدید وضعیت عملکرد سیستم های قلبی، تنفسی و عضلانی استخوانی و تغییر در روند پیشرفت بیماری است.1,26 جدای از ERT، ارزیابی های جامع منظم، درمان نشانه ای و مداخله ای جراحی،1,7 استمرار مراقبت ها از دوره کودکی تا بزرگسالی جزو ملاحظات بسیار مهم برای بیماران مبتلا به MPS و خانواده های آنها می باشد.1,30
بیماران مبتلا به MPS IV برای رفع عوارض مولتی سیستمیک ناشی از بیماری اغلب به مداخله جراحی نیاز پیدا می کنند.7 این مراقبت های جراحی به دلیل ماهیت بیماری پیچیده می شوند.
بیماران مبتلا به MPS IV از عوامل مختلفی رنج می برند که می تواند خطر جراحی را شدیداً افزایش داده و نیاز به نظارت را ایجاد می نماید:33
این عوامل باعث پیچیده شدن مراقبت های جراحی و بیهوشی شده و نیاز به پیش برنامه ریزی و تکنیک های خاص این بیماری را برای بالا بردن احتمال بهینه بودن نتایج کار ایجاد می نمایند.33
روال های تخصصی پیش از عمل در طول بیهوشی، مانند لوله گذاری و برداشتن لوله، و استفاده از چک لیست مونیتورینگ عصبی در حین عمل، برای موفقیت مداخله های جراحی ضروری هستند.1,33 وجود یک گروه یکپارچه جراحی متشکل از متخصصان MPS VI برای مثبت و ماندگار بودن نتایج از اهمیت بسزائی برخوردار است.1
با رسیدن بیماران مبتلا به MPS IV به دوره بزرگسالی، رابطه آنها با گروه پزشکی تغییر خواهد کرد. برای کمک در مدیریت این انتقال به برنامه های اختصاصی و فردی نیاز خواهد بود تا وقفه های درمانی به حداقل ممکن کاهش داده شده، پشتیبانی ها فراتر از ابعاد مراقبت های اطفال و حمایت های والدین گسترش داده شده و این اطمینان بوجود آید که بیماران در زمینه مدیریت MPS IV دارای اطلاعات و آگاهی هستند.1,30
این برنامه های انتقالی باید بر اساس نیازهای خاص هر بیمار تهیه شوند. بدین ترتیب آنهائی که می توانند مراقبت های خود را بر عهده بگیرند از ابزارهای لازم برخوردار شده و آنهائی که محدودتر هستند می توانند از مراقبت ها و حمایت های لازم بهره مند گردند. برنامه ها باید شامل یک ارزیابی جهت مشخص ساختن ظرفیت بیمار در دست یافتن به اهداف مشخص شده و نیز توانائی و دانش وی برای بیان وضعیت و حالت عارضه خود باشد.30
References: 1. Hendriksz CJ et al. International guidelines for the management and treatment of Morquio A syndrome. Am J Med Genet Part A 2014;9999A:1–15. 2. Northover H et al. Mucopolysaccharidosis type IVA (Morquio syndrome): a clinical review. J Inherit Metab Dis 1996;19(3):357–365. 3. Islam T et al. Chemistry, biochemistry, and pharmaceutical potentials of glycosaminoglycans and related saccharides. In: Wong C-H, ed. Carbohydrate-based Drug Discovery Weinheim, Germany: WILEY-VCH Verlag GmbH & Co KGaA; 2003:407–439. 4. Tomatsu S et al. Mutation and polymorphism spectrum of the GALNS gene in mucopolysaccharidosis IVA (Morquio A). Hum Mutat 2005;26(6):500–512. 5. Montaño AM et al.International Morquio A Registry: clinical manifestation and natural course of Morquio A disease. J Inherit Metab Dis 2007;30(2):165-174. 6. Tomatsu S et al. Mucopolysaccharidosis type IVA (Morquio A disease): clinical review and current treatment: a special review. Curr Pharm Biotechnol 2011;12(6):931–945. 7. Harmatz P et al. The Morquio A clinical assessment program: baseline results illustrating progressive, multisystemic clinical impairments in Morquio A subjects. Mol Genet Metab 2013;109(1):54–61. 8. John RM et al. Echocardiographic abnormalities in type IV mucopolysaccharidosis. Arch Dis Child 1990;65(7):746–749. 9. Ireland MA, Rowlands DB. Mucopolysaccharidosis type IV as a cause of mitral stenosis in an adult. Br Heart J 1981;46(1):113–115. 10. Semenza GL, Pyeritz RE. Respiratory complications of mucopolysaccharide storage disorders. Medicine 1988;67(4):209–219. 11. Pelley CJ et al. Tracheomalacia in an adult with respiratory failure and Morquio syndrome. Respir Care 2007;52(3):278–282. 12. Gulati MS et al. Morquio syndrome: a rehabilitation perspective. J Spinal Cord Med 1996;19(1):12–16. 13. Holzgreve W et al. Morquio syndrome: clinical findings in 11 patients with MPS IVA and 2 patients MPS IVB. Hum Genet 1981;57(4):360–365. 14. Danes BS. Corneal clouding in the genetic mucopolysaccharidoses: a cell culture study. Clin Genet 1973;4(1):1–7. 15. Leslie T et al. Morquio syndrome: electron microscopic findings [letter]. Br J Ophthalmol 2005;89(7):917–929. 16. Hendriksz CJ et al. Review of clinical presentation and diagnosis of mucopolysaccharidosis IVA. Mol Genet Metab 2013;110:54–64. 17. Kinirons MJ, Nelson J. Dental findings in mucopolysaccharidosis type IV A (Morquio's disease type A). Oral Surg Oral Med Oral Pathol 1990;70(2):176–179. 18. Data on file. BioMarin Pharmaceutical Inc. 19. Berger KI et al. Respiratory and sleep disorders in mucopolysaccharidosis. J Inherit Metab Dis 2013;36(2):201–210. 20. Hendriksz C. Improved diagnostic procedures in attenuated mucopolysaccharidosis. Br J Hosp Med 2011;72(2):91–95. 21. Clarke LA. Pathogenesis of skeletal and connective tissue involvement in the mucopolysaccharidoses: glycosaminoglycan storage is merely the instigator. Rheumatology (Oxford) 2011;50(suppl 5):v13–18. 22. Lehman TJA et al. Diagnosis of the mucopolysaccharidoses. Rheumatology 2011;50(suppl 5):v41–v48. 23. Morishita K, Petty RE. Musculoskeletal manifestations of mucopolysaccharidoses. Rheumatology 2011;50(suppl 5):v19–v25. 24. Muenzer J. Overview of the mucopolysaccharidoses. Rheumatology (Oxford). 2011;50(suppl 5):v4–v12. 25. Wood TC et al. Diagnosing mucopolysaccharidosis IVA. J Inherit Metab Dis 2013;36(2):293–307. 26. VIMIZIM [package insert]. Novato, CA: BioMarin Pharmaceutical Inc; 2014. 27. Coutinho MF et al. Glycosaminoglycan storage disorders: a review. Biochem Res Int 2012;2012:471325. 28. Bank RA et al. Deficiency in N-acetylgalactosamine-6-sulfate sulfatase results in collagen perturbations in cartilage of Morquio syndrome A patients. Mol Genet Metab 2009;97(3):196–201. 29. Harmatz P et al. Longitudinal analysis of endurance and respiratory function from a natural history study of Morquio A syndrome. Mol Genet Metab 2015;114(2):186–194. 30. American Academy of Pediatrics, American Academy of Family Physicians, American College of Physicians, Transitions Clinical Report Authoring Group, Cooley WC, Sagerman PJ. Supporting the health care transition from adolescence to adulthood in the medical home. Pediatrics 2011;128(1):182–200. 33. Walker R et al. Anaesthesia and airway management in mucopolysaccharidosis. J Inherit Metab Dis 2013;36(2):211–219. 33. Theroux MC et al. Anesthetic care and perioperative complications of children with Morquio syndrome. Paediatr Anaesth 2012;22(9):901–907.