
Onlarca yıldır süren araştırmalar ve klinik deneyim, mukopolisakkaridoz (MPS) hastalıklarının en uygun yönetiminde yeni bir çağ açmıştır. MPS için hızla gelişen bu standart bakım, koordineli, multidisipliner bir bakımı bünyesinde barındıran ve hekimlere hastaların yaşamlarını değiştirmek için eşsiz fırsatlar sağlayan bir sağlık hizmeti sunma modelinin merkezindeki metabolizma veya genetik uzmanına dayanmaktadır.1–3
MPS hastalıkları çok çeşitli merkezi ve periferik sinir sistemi anomalileriyle ilişkili olduğundan dolayı, nörologlar bu hastaların devam eden değerlendirmesi ve yönetiminde kritik bir rol oynamaktadır ve devam eden bakımlarına önemli ölçüde katkı sağlayabilirler.1,4–7
MPS hastalıklarının heterojen ve değişken doğası, koordineli hasta bakımı için evde sağlık hizmetiyle başlayan, kişiselleştirilmiş bir yaklaşım gerektirmektedir.1 Koordineli bakımın amacı, aşağıdakiler de dahil olmak üzere hastaların daha yüksek bir yaşam kalitesini elde etmelerine yardımcı olmaktır:
MPS gibi kronik, karmaşık, multisistemik genetik hastalığı olan pediyatrik hastalar için koordineli evde sağlık hizmeti aracılığıyla bakım, sağlık hizmetlerinin kullanımının azaltılması ve sağlık sonuçlarının iyileştirilmesi ile ilişkilidir.8-11
Koordinasyon, geniş sağlık sisteminin tüm unsurları (örn. özel bakım, hastaneler, evde sağlık hizmeti ve toplum hizmetleri) ve hastaların bireyselleştirilmiş yönetim planları dahilinde uygulanmalıdır.3 Çok çeşitli merkezi ve periferik sinir sistemi anomalileri göz önüne alındığında, nörologların evde sağlık hizmetine dair rolü, MPS hastalıklarının yönetiminde ve hasta sonuçlarının iyileştirilmesinde en iyi uygulamaların tatbik edilmesi için vazgeçilmez olabilir.1,2
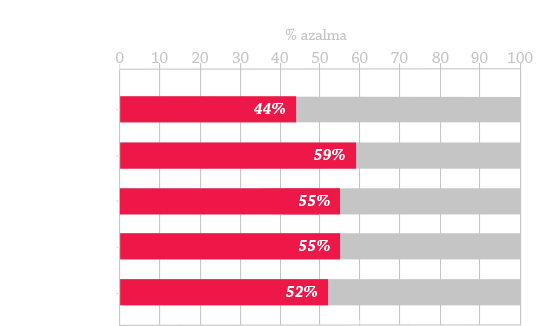
Aşağıda 3 tedavi desteği olarak gruplanmış en uygun MPS hastalığı yönetiminin uygulanması, hasta sonuçlarını iyileştirmeye yardımcı olabilir:
Nörologlar, koordineli bir yaklaşımın bir parçası olarak ömür boyu yönetimi ve prosedürel bakımı ele alan, bireyselleştirilmiş yönetim planlarına katkıda bulunmakta ve sonuç olarak hastanın sonuçlarını en iyi duruma getirmeye yardımcı olmaktadır.1,4–7
Yapılabiliyorsa ERT, tedavinin temel taşıdır.12-14
MPS hastalığının her bir alt tipi klinik açıdan birbirinden farklı olsa da, hepsi MPS hastalığının patolojisinde yaygın olarak görülen, yaşamı sınırlayan, progresif, multisistemik hastalık bulguları ortaya koymaktadır.14,15,23,24 MPS'li hastaların yönetiminde, her bir MPS alt tipi için belirli klinik bulguların ve yönetim tavsiyelerinin anlaşılması gerekmektedir.2,13
I
II
(A, B, C ve D)
α-N-asetilglukozaminidaz, Asetil CoA:
α-glukozaminidN-asetiltransferaz, N-asetilglukozamin-6-sülfataz
IV
β-galaktosidaz
VI(A ve B)
VII(A ve B)
IX
Kasım 2015
Birçok düzenlemeye rağmen, en uygun bilateral doğum sancısı analjezisi sağlanamamış ve sezaryen doğum için sistemik analjeziye ihtiyaç duyulmuştur.
Mayıs 2015
Tanı tesislerinin mevcut olmaması veya uzak olması, alternatif tanılar ve yaşanan yanıltıcı semptomlar nedeniyle, tanıda gecikmeler meydana gelmiştir. Birçok hasta beklenenden daha gizli olan ve bunu takiben göz ardı edilen bulgular yaşamıştır. Vakalar ayrıca, MPS VI'nın farklı uzmanlık dalları açısından tanılanmasıyla ilişkili benzersiz zorlukları vurgulamıştır ve bu hastalarda ilk belirtilerin nasıl görüldüğü konusunda fikirler vermektedir.
Nisan 2016
Özellikle koroner dolaşım ve miyokard sorunu bulunan MPS'li yetişkinlerdeki diğer kalp sorunlarına dair mevcut anlayışımız yetersizdir ve bu öne çıkan yetişkin popülasyonuna etkili şekilde bakım sunmak için daha fazla bilgiye ihtiyaç vardır.
Referanslar: 1. Hendriksz CJ et al. International guidelines for the management and treatment of Morquio A syndrome. Am J Med Genet Part A. 2014;9999A:1–15; 2. Muenzer J. The mucopolysaccharidoses: a heterogeneous group of disorders with variable pediatric presentations. J Pediatr. 2004;144(suppl 5):S27–S34. 3. Agency for Healthcare Research and Quality. Defining the PCMH. https://pcmh.ahrq.gov/page/defining-pcmh. Accessed December 15, 2015. 4. Zafeiriou DI et al. Brain and spinal MR imaging findings in mucopolysaccharidoses: a review. AJNR Am J Neuroradiol. 2013;34(1):5–13; 5. Solanki GA et al. Spinal involvement in mucopolysaccharidosis IVA (Morquio-Brailsford or Morquio A syndrome): presentation, diagnosis and management. J Inherit Metab Dis. 2013;36(2):339–355; 6. Kakkis ED et al. The mucopolysaccharidoses. In: Berg BO, ed. Principles of Child Neurology. New York, NY: McGraw-Hill; 1996:1141–1166. 7. Lachman R et al. Radiologic and neuroradiologic findings in the mucopolysaccharidoses. J Pediatr Rehabil Med. 2010;3(2):109–118. 8. Casey PH et al. Effect of hospital-based comprehensive care clinic on health costs for Medicaid-insured medically complex children. Arch Pediatr Adolesc Med. 2011;165(5):392–398. 9. Mosquera RA et al. Effect of an enhanced medical home on serious illness and cost of care among high-risk children with chronic illness: a randomized clinical trial. JAMA. 2014;312(24):2640–2648. 10. Klitzner TS et al. Benefits of care coordination for children with complex disease: a pilot medical home project in a resident teaching clinic. J Pediatr. 2010;156(6):1006–1010. 11. Gordon JBet al.. A tertiary care-primary care partnership model for medically complex and fragile children and youth with special health care needs. Arch Pediatr Adolesc Med. 2007;161(10):937–944. 12. Hendriksz C. Improved diagnostic procedures in attenuated mucopolysaccharidosis. Br J Hosp Med. 2011;72(2):91–95. 13. Muenzer J et al. International Consensus Panel on the Management and Treatment of Mucopolysaccharidosis I. Mucopolysaccharidosis I: management and treatment guidelines. Pediatrics. 2009;123(1):19–29. 14. Muenzer J et al.Long-term, open-labeled extension study of idursulfase in the treatment of Hunter syndrome. Genet Med. 2011;13(2):95–101. 15. Lehman TJA et al. Diagnosis of the mucopolysaccharidoses. Rheumatology. 2011;50(suppl 5):v41–v48. 16. Lavery C et al. Mortality in patients with Morquio syndrome A. J Inherit Metab Dis Rep. 2015;15:59–66. 17. Giugliani R et al. Natural history and galsulfase treatment in mucopolysaccharidosis VI (MPS VI, Maroteaux-Lamy syndrome) – 10-year follow-up of patients who previously participated in an MPS VI Survey Study. Am J Med Genet A. 2014;164A(8):1953–1964. 18. Spinello CM et al. Anesthetic management in mucopolysaccharidoses. ISRN Anesthesiol. 2013;2013:1–10. 19. Sam JA et al. Mucopolysaccharidoses: anesthetic considerations and clinical manifestations. Middle East J Anaesthesiol. 2011;21(2):243–253. 20. Data on file. Biomarin Pharmaceutical Inc. 21. Drummond JC et al. Paraplegia after epidural-general anesthesia in a Morquio patient with moderate thoracic spinal stenosis. Can J Anesth. 2015;62(1):45–49. 22. Sharkia R et al. Sanfilippo type A: new clinical manifestations and neuro-imaging findings in patients from the same family in Israel: a case report. J Med Case Rep. 2014;8:78. 23. Clarke LA et al. ńska A, Amartino H. Biomarkers for the mucopolysaccharidoses: discovery and clinical utility. Mol Genet Metab. 2012;106(4):396–402. 24. Morishita K et al.. Musculoskeletal manifestations of mucopolysaccharidoses. Rheumatology. 2011;50(suppl 5):v19-v25. d