
Результаты исследований сибсов подтверждают, что своевременное поставленный диагноз улучшает прогноз клинического течения заболевания у пациентов за счет адекватной тактики лечения и своевременного начала ФЗТ, при наличии такой возможности.1-6
Было показано, что начало ФЗТ как на ранних так и на более поздних этапах жизни улучшает основные клинические параметры, такие как выносливость и функция внешнего дыхания, показатели функции легких, которые имеют решающее значение для качества жизни, поддержания способности к передвижению и ежедневной активности.7,8
Вы покидаете сайт MPSReference. Пожалуйста, выберите ссылку ниже, чтобы получить дополнительную информацию о конкретных доступных видах ферментной заместительной терапии.
Vimizim.com– лечение синдрома Моркио A
Naglazyme.com– лечение МПС VI
Дополнительную информацию о клинических испытаниях можно найти на сайте www.clinicaltrials.gov.
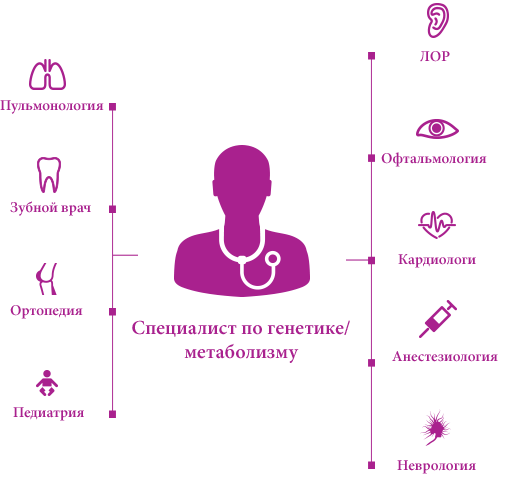
В новую эру лечения прогрессирующих комплексных генетических заболеваний, таких как мукополисахаридозы (МПС), всё зависит от эффективной координации деятельности каждой группы врачей, работающих с пациентом.1
Обычно в медицинском учреждении есть специалисты-генетики – они помогают скоординировать работу многопрофильной группы врачей и составить индивидуальный план лечения.2,3
Учитывая большое количество хирургических вмешательств у пациентов с МПС, что является следствием системного характера заболевания, анестезиологи и операционная бригада играют важную роль в мультидисциплинарной команде.4,5

Для МПС различных типов разработаны протоколы ведения пациентов и специализированные рекомендации по непрерывному лечению МПС. Рекомендации как правило включают:3,6
Своевременно и регулярно проводимая группой специалистов оценка состояния пациента способна продемонстрировать результаты лечения и способствовать предотвращению необратимых последствий.6
Поражения скелета и мультисистемые проявления МПС повышают риски пред- и послеоперационных осложнений и смертности.5,8
Обструкция дыхательных путей и отек легких – одни из наиболее грозных осложнений, связанных с проведением анестезии, которые в некоторых случаях требуют экстренной трахеостомии или повторной интубации и могут быть чрезвычайно сложными.5
Пациенты с МПС подвержены повышенному риску осложнений при проведении анестезии и премедикации. По возможности следует избегать общей анестезии; если такая необходимость есть, выполнять процедуру должны только опытные анестезиологи.8,9
Оценка рисков, связанныхе с седациейе и общей анестезиейя, вляется критическим фактором при выборе метода визуализации для оценки поражения позвоночника.8
Специалистам, осуществляющим анестезиологическое пособие у пациентов с МПС, необходимо учитывать специфические системные осложнения, характерные для различных типов МПС, особенно проявления компрессии спинного мозга и обструкции дыхательных путей.8
Подготовка пациентов с МПС с учётом хирургического и анестетического рисков требует слаженной работы опытной группы врачей разных специальностей, в которую входят анестезиолог, кардиолог, пульмонолог и отоларинголог.5
К факторам анестезиологического риска относятся следующие:
Соблюдение рекомендаций по интраоперационной терапии при работе скоординированной группы имеют решающее значение для снижения вероятности отрицательных результатов хирургического лечения.5 Эти рекомендации приводятся в таблице ниже.
Анестезиологический риск у пациентов с МПС считается высоким по многим причинам, в том числе из-за поражения дыхательных путей, скелетных деформаций, предрасположенности к легочным заболеваниям и поражению сердца и ЦНС.9 Следует отметить, что для некоторых типов МПС характерны более высокие риски по сравнению с другими типами (см. таблицу ниже).
Подтип и степень тяжести МПС являются важными индикаторами анестезиологического риска и должны быть оценены до проведения операции. Интраоперационный риск выше у пациентов с МПС I, II, IV и VI типов прис общем показателе общей смертности до 20%9
Частота проведения обследований и участие конкретных специалистов различаются в зависимости от типа МПС. Для пациентов МПС с первичными нейродегенеративными и когнитивными осложнениями, например с МПС I, II и III типов, рекомендуется проведение дополнительного и регулярного нейробиологического и психиатрического обследования6,12,13
В дополнение к специализированным обследованиям, которые способствуют улучшению долгосрочных результатов у пациентов с МПС, лечащий врач, как правило, генетик, может предпринять важные меры по улучшению, общего состояния здоровья. Функции этих специалистов имеют решающее значение в информировании врачей других специальностей (например, стоматологов, физиотерапевтов, педиатров, семейных врачей) и членов семей пациентов о специфике заболевания и общих стратегиях лечения и должны включать3:
Специализированное обследование, регулярные медицинские осмотры и общетерапевтические методы лечения должны выполняться в соответствии с клиническими рекомендациями, которые могут отличаться в зависимости от типов МПС.3
Совершенствование методов лечения МПС способствует улучшению долгосрочных результатов пациентов, что требует новых подходов к лечению на протяжении всей жизни.
По мере взросления некоторые пациенты могут взять на себя функцию по самостоятельному контролю за собственным здоровьем. Следовательно, важное значение приобретает передача пациента во взрослую сеть при активном участии лечащего врача.3 Врачи должны обеспечить следующие условия:
Процесс перевода пациентов из педиатрической сети во взрослую и непрерывное в долгосрочной перспективе – являются важнейшими элементами, которые необходимо учитывать при составлении индивидуальных планов лечения для пациентов подросткового возраста и взрослых пациентов.3 Наилучшими возможностями для обеспечения долгосрочного лечения медицинские центры опытом работы с МПС, поскольку требуется чёткая координация действий со стороны врачей разных специальностей.3,15 Процесс обеспечения долгосрочного лечения включает следующие аспекты (но не ограничиваются ими):
Лечение пациентов с МПС в долгосрочной перспективе, включающее проведение регулярных обследовани и реализующее стратегию перевода из педиатрической сети во взрослую, может обеспечить значительное улучшение качества жизни и лучший прогноз в отношение будущегое ваших пациентов.3,15-17
Поскольку клинические проявления мукополисахаридозов являются полиорганными, необходимо применять многопрофильный индивидуальный подход к каждому пациенту, с целью активного выявления и коррекции возникающих осложнений. Анестезия должна проводиться опытными анестезиологами и обученным персоналом исключительно в специализированных центрах. Окончательное решение о проведении операции должно приниматься только после консультации анестезиолога, который возьмет на себя обязательства по обсуждению потенциальных рисков и пользы с пациентами и их семьями1
Пациентам с МПС в течение жизни, как правило проводят целый ряд хирургических вмешательств. Исследование естественного течения заболевания, в котором оценивалась выборка из 325 пациентов с синдромом Моркио A (МПС IVA), показало, что у более 70% пациентов было проведено по крайней мере одно хирургическое вмешательство2

Для пациентов с МПС характерны высокие показатели периоперационной смертности в связи с большим количеством факторов, включая обструкцию верхних и нижних дыхательных путей, нестабильность шейного отдела позвоночника, нарушение дыхания, сердечно-сосудистую патологию и частые инфекции2-4. Так, в результате хирургических осложнений смертность пациентов с синдромом Моркио A составила 11% (n = 27).5
Решающее значение имеет реализация разработанного плана проведения хирургических вмешательств, включающегоее работу мультидисциплинарной команды специалистов, которая имеет опыт лечения пациентов с МПС3
Поскольку у пациентов с МПС повышен риск развития анестезиологических и хирургических осложнений, большое значение имеет информированность о передовых методах подготовки к хирургическим вмешательствам и особенностях перед- и послеоперационной помощи пациентам с МПС. Стандартная предоперационная подготовка является недостаточной и неэффективной для пациентов с МПС. Для успешного планирования и проведения процедур, необходимых для обеспечениях анестезии, должна проводиться всесторонняя оценка каждого конкретного клинического случая1.
Необходимо осуществлять послеоперационный контроль и тщательно проводить повторные обследования, даже если пациенты демонстрируют устойчивое улучшение в течение первого года после хирургической операции, поскольку последующее накопление гликозаминогликанов (ГАГ) может оказывать влияние на анатомию дыхательных путей, а также сердечную и легочную функции1.
Для точного предоперационного обследования требуется проведение ряда анализов1:
Общая анестезия опасна и в целом ее следует избегать: предпочтительной является местная анестезия методомс периферической блокады. Кроме того, с целью снижения рисков, связанных с воздействием нескольких анестетиков, рекомендуется объединять два или более диагностических/хирургических вмешательства в течение одной анестезии1.
Послеоперационная терапия включает в себя использование стероидовс целью уменьшения отека, стандартную терапию для пациентов с обструкцией верхних дыхательных путей (применение устройств постоянной или двухфазной вентиляции с положительным давлением в дыхательных путях) и непрерывный контроль показателей респираторной и сердечной функций1.
В случае необходимости экстренного хирургического вмешательства следует соблюдать рекомендации для пациентов с подозрением на травмы шейного отдела позвоночника1.
Оценка рисков хирургического вмешательства и периоперационный мониторинг являются фундаментальной основой индивидуального хирургического плана. Кроме того, это может снизить риск отрицательных результатов хирургического лечения и смертности у пациентов с МПС 3,9,10.
References: 1. McGill JJ, Inwood AC, Coman DJ, et al. Enzyme replacement therapy for mucopolysaccharidosis VI from 8 weeks of age—a sibling control study. Clin Genet. 2010;77(5):492–498. doi:10.1111/j.1399-0004.2009.01324.x. 2. Furujo M, Kubo T, Kosuga M, Okuyama T. Enzyme replacement therapy attenuates disease progression in two Japanese siblings with mucopolysaccharidosis type VI. Mol Genet Metab. 2011;104(4):597–602. doi:10.1016/j.ymgme.2011.08.029. 3. Clarke LA. Pathogenesis of skeletal and connective tissue involvement in the mucopolysaccharidoses: glycosaminoglycan storage is merely the instigator. Rheumatology (Oxford). 2011;50(suppl 5):v13–18. 4. Lehman TJA, Miller N, Norquist B, Underhill L, Keutzer J. Diagnosis of the mucopolysaccharidoses. Rheumatology. 2011;50(suppl 5):v41–v48. 5. Morishita K, Petty RE. Musculoskeletal manifestations of mucopolysaccharidoses. Rheumatology. 2011;50(suppl 5):v19–v25. doi:10.1093/rheumatology/ker397. 6. Muenzer J, Beck M, Eng CM, et al.Genet Med. 2011;13(2):95–101. doi:10.1097/GIM.0b013e3181fea459. 7. Hendriksz C. Improved diagnostic procedures in attenuated mucopolysaccharidosis. Br J Hosp Med. 2011;72(2):91-95. 8. Muenzer J. Early initiation of enzyme replacement therapy for the mucopolysaccharidoses. Mol Genet Metab. 2014;111(2):63–72. doi:10.1016/j.ymgme.2013.11.015. 9. Hendriksz CJ, Berger KI, Giugliani R, et al. International guidelines for the management and treatment of Morquio A syndrome. Am J Med Genet Part A. 2014;9999A:1–15. doi:10.1002/ajmg.a.36833. 10. Bagewadi S, Roberts J, Mercer J, Jones S, Stephenson J, Wraith JE. Home treatment with Elaprase® and Naglazyme® is safe in patients with mucopolysaccharidoses types II and VI, respectively. J Inherit Metab Dis. 2008;31(6):733–737. doi:10.1007/s10545-008-0980-0. 11. BioMarin Pharmaceutical Inc. VIMIZIM Web site. http://www.vimizim.com/. Accessed December 21, 2015. 12. BioMarin Pharmaceutical Inc. Naglazyme Web site. http://www.naglazyme.com/. Accessed December 21, 2015. 13. Muenzer J, Wraith JE, Clarke LA, International Consensus Panel on the Management and Treatment of Mucopolysaccharidosis I. Mucopolysaccharidosis I: management and treatment guidelines. Pediatrics. 2009;123(1):19–29. doi:10.1542/peds.2008-0416.
References: 1. Agency for Healthcare Research and Quality. Defining the PCMH. https://pcmh.ahrq.gov/page/defining-pcmh. Accessed December 15, 2015. 2. Muenzer J. The mucopolysaccharidoses: a heterogeneous group of disorders with variable pediatric presentations. J Pediatr. 2004;144(suppl 5):S27–S34. 3. Hendriksz CJ, Berger KI, Giugliani R, et al. International guidelines for the management and treatment of Morquio A syndrome. Am J Med Genet Part A. 2014;9999A:1–15. doi:10.1002/ajmg.a.36833. 4. Harmatz P, Mengel KE, Giugliani R, et al. The Morquio A clinical assessment program: baseline results illustrating progressive, multisystemic clinical impairments in Morquio A subjects. Mol Genet Metab. 2013;109(1):54–61. doi:10.1016/j.ymgme.2013.01.021. 5. Walker R, Belani KG, Braunlin EA, et al. Anaesthesia and airway management in mucopolysaccharidosis. J Inherit Metab Dis. 2013;36(2):211–219. doi:10.1007/s10545-012-9563-1. 6. Muenzer J, Wraith JE, Clarke LA, International Consensus Panel on the Management and Treatment of Mucopolysaccharidosis I. Mucopolysaccharidosis I: management and treatment guidelines. Pediatrics. 2009;123(1):19–29. doi:10.1542/peds.2008-0416. 7. Vitale MG, Skaggs DL, Pace GI, et al. Delphi Consensus Report: Best practices in intraoperative neuromonitoring in spine deformity surgery: development of an intraoperative checklist to optimize response. Spine Deformity. 2014;2(5):333–339. doi:10.1016/j.jspd.2014.05.003. 8. Solanki GA, Martin KW, Theroux MC, et al. Spinal involvement in mucopolysaccharidosis IVA (Morquio-Brailsford or Morquio A syndrome): presentation, diagnosis and management. J Inherit Metab Dis. 2013;36(2):339–355. doi:10.1007/s10545-013-9586-2. 9. Spinello CM, Novello LM, Pitino S, et al. Anesthetic management in mucopolysaccharidoses. ISRN Anesthesiol. 2013;2013:1–10. doi:10.1155/2013/791983. 10. Theroux MC, Nerker T, Ditro C, Mackenzie WG. Anesthetic care and perioperative complications of children with Morquio syndrome. Paediatr Anaesth. 2012;22(9):901–907. doi:10.1111/j.1460-9592.2012.03904.x. 11. Solanki GA, Alden TD, Burton BK, et al. A multinational, multidisciplinary consensus for the diagnosis and management of spinal cord compression among patients with mucopolysaccharidosis VI. Mol Genet Metab. 2012;107:15–24. doi:10.1016/j.ymgme.2012.07.018. 12. Neufeld EF, Muenzer J. The mucopolysaccharidoses. In: Scriver CR, Beaudet AL, Sly WS, Valle D, eds. The Metabolic and Molecular Bases of Inherited Disease. Vol 3. 8th ed. New York: McGraw-Hill; 2002:2465–2494. 13. Scarpa M, Almassy Z, Beck M, et al. Mucopolysaccharidosis type II: European recommendations for the diagnosis and multidisciplinary management of a rare disease. Orphanet J Rare Dis. 2011;6:72. doi:10.1186/1750-1172-6-72. 14. James A, Hendriksz CJ, Addison O. The oral health needs of children, adolescents and young adults affected by a mucopolysaccharide disorder. JIMD Rep. 2012;2:51–58. doi:10.1007/8904_2011_46. 15. Coutinho MF, Lacerda L, Alves S. Glycosaminoglycan storage disorders: a review. Biochem Res Int. 2012;2012:471325. doi:10.1155/2012/471325. 16. Kakkis ED, Neufeld EF. The mucopolysaccharidoses. In: Berg BO, ed. Principles of child neurology. New York, NY: McGraw-Hill; 1996:1141–1166. 17. Lehman TJA, Miller N, Norquist B, Underhill L, Keutzer J. Diagnosis of the mucopolysaccharidoses. Rheumatology. 2011;50(suppl 5):v41-v48.
References: 1. Spinello CM, Novello LM, Pitino S, et al. Anesthetic management in mucopolysaccharidoses. ISRN Anesthesiol. 2013;2013:1–10. doi:10.1155/2013/791983. 2. Harmatz P, Mengel KE, Giugliani R, et al. The Morquio A clinical assessment program: baseline results illustrating progressive, multisystemic clinical impairments in Morquio A subjects. Mol Genet Metab. 2013;109(1):54–61. doi:10.1016/j.ymgme.2013.01.021. 3. Walker R, Belani KG, Braunlin EA, et al. Anaesthesia and airway management in mucopolysaccharidosis. J Inherit Metab Dis. 2013;36(2):211–219. doi:10.1007/s10545-012-9563-1. 4. Hendriksz CJ, Berger KI, Giugliani R, et al. International guidelines for the management and treatment of Morquio A syndrome. Am J Med Genet Part A. 2014;9999A:1–15. doi:10.1002/ajmg.a.36833. 5. Lavery C, Hendriksz C. Mortality in patients with Morquio syndrome A. J Inherit Metab Dis Rep. 2015;15:59–66. doi:10.1007/8904_2014_298. 6. Theroux MC, Nerker T, Ditro C, Mackenzie WG. Anesthetic care and perioperative complications of children with Morquio syndrome. Paediatr Anaesth. 2012;22(9):901–907. doi:10.1111/j.1460-9592.2012.03904.x. 7. Muenzer J. The mucopolysaccharidoses: a heterogeneous group of disorders with variable pediatric presentations. J Pediatr. 2004;144(suppl 5):S27–S34. 8. Scarpa M, Almassy Z, Beck M, et al. Mucopolysaccharidosis type II: European recommendations for the diagnosis and multidisciplinary management of a rare disease. Orphanet J Rare Dis. 2011;6:72. doi:10.1186/1750-1172-6-72. 9. Solanki GA, Martin KW, Theroux MC, et al. Spinal involvement in mucopolysaccharidosis IVA (Morquio-Brailsford or Morquio A syndrome): presentation, diagnosis and management. J Inherit Metab Dis. 2013;36(2):339–355. doi:10.1007/s10545-013-9586-2. 10. Vitale MG, Skaggs DL, Pace GI, et al. Delphi Consensus Report: Best practices in intraoperative neuromonitoring in spine deformity surgery: development of an intraoperative checklist to optimize response. Spine Deformity. 2014;2(5):333–339. doi:10.1016/j.jspd.2014.05.003.